Pasaulis, kuriame gyvename, yra neįsivaizduojamai gražus ir pilnas daugybės skirtingų procesų, kurie nustato gyvenimo eigą. Visus šiuos procesus tiria pažįstamas mokslas - fizika. Tai suteikia galimybę bent šiek tiek įsivaizduoti visatos kilmę. Šiame straipsnyje mes apsvarstysime tokią sąvoką kaip molekulinė kinetinė teorija, jos lygtis, tipus ir formules. Tačiau prieš pereidami prie gilesnio šių klausimų tyrimo, turite patys išsiaiškinti fizikos ir jos tyrinėjamų sričių prasmę.
Kas yra fizika?

Tiesą sakant, tai labai platus mokslas ir, ko gero, vienas svarbiausių žmonijos istorijoje. Pavyzdžiui, jei tas pats kompiuterių mokslas yra susijęs su beveik visomis žmogaus veiklos sritimis, nesvarbu, ar tai būtų kompiuterinis dizainas, ar animacinių filmų kūrimas, tada fizika yra pats gyvenimas, jo sudėtingų procesų ir srautų aprašymas. Pabandykime išsiaiškinti jo reikšmę, kiek įmanoma supaprastindami supratimą.
TaigiTaigi, fizika yra mokslas, nagrinėjantis energiją ir materiją, ryšius tarp jų, daugelio mūsų didžiulėje visatoje vykstančių procesų paaiškinimą. Molekulinė-kinetinė materijos sandaros teorija yra tik mažas lašelis teorijų ir fizikos šakų jūroje.
Energija, kurią šis mokslas išsamiai tiria, gali būti pavaizduota įvairiomis formomis. Pavyzdžiui, šviesos, judesio, gravitacijos, spinduliuotės, elektros ir daugelio kitų formų pavidalu. Šiame straipsnyje paliesime molekulinę kinetinę šių formų struktūros teoriją.
Materijos tyrimas suteikia supratimą apie materijos atominę struktūrą. Beje, tai išplaukia iš molekulinės-kinetinės teorijos. Materijos sandaros mokslas leidžia suprasti ir rasti savo egzistencijos prasmę, gyvybės atsiradimo priežastis ir pačią Visatą. Dar pabandykime ištirti molekulinę kinetinę materijos teoriją.
Pirma, reikia šiek tiek įvado, kad būtų visiškai suprantama terminija ir visos išvados.
Fizikos temos
Atsakant į klausimą, kas yra molekulinė-kinetinė teorija, galima nekalbėti apie fizikos dalis. Kiekvienas iš jų yra susijęs su išsamiu tam tikros žmogaus gyvenimo srities tyrimu ir paaiškinimu. Jie klasifikuojami taip:
- Mechanika, kuri suskirstyta į dar dvi dalis: kinematika ir dinamika.
- Statinis.
- Termodinamika.
- Molekulinė pjūvis.
- Elektrodinamika.
- Optika.
- Kvantų ir atomo branduolio fizika.
Pakalbėkime konkrečiai apie molekulinęfizika, nes ji pagrįsta molekuline-kinetine teorija.
Kas yra termodinamika?
Apskritai, molekulinė dalis ir termodinamika yra glaudžiai susijusios fizikos šakos, kurios tiria tik makroskopinį viso fizinių sistemų skaičiaus komponentą. Verta prisiminti, kad šie mokslai tiksliai apibūdina vidinę kūnų ir medžiagų būseną. Pavyzdžiui, jų būsena kaitinimo, kristalizacijos, garavimo ir kondensacijos metu atominiame lygmenyje. Kitaip tariant, molekulinė fizika yra mokslas apie sistemas, susidedančias iš daugybės dalelių: atomų ir molekulių.
Būtent šie mokslai tyrė pagrindines molekulinės kinetinės teorijos nuostatas.
Dar septintoje klasėje susipažinome su mikro ir makro pasaulių, sistemų sampratomis. Nebus nereikalinga atnaujinti šiuos terminus atmintyje.
Mikropasaulis, kaip matome iš paties pavadinimo, susideda iš elementariųjų dalelių. Kitaip tariant, tai yra mažų dalelių pasaulis. Jų dydžiai matuojami diapazone nuo 10-18 m iki 10-4 m, o tikrosios būsenos laikas gali siekti ir begalybę, ir neproporcingai mažais intervalais, pavyzdžiui, 10-20 s.
Makropasaulis laiko stabilių formų kūnus ir sistemas, sudarytas iš daugelio elementariųjų dalelių. Tokios sistemos atitinka mūsų žmogaus dydį.
Be to, yra toks dalykas kaip mega pasaulis. Jį sudaro didžiulės planetos, kosminės galaktikos ir kompleksai.
Pagrindaiteorija
Dabar, kai šiek tiek apibendriname ir prisiminėme pagrindinius fizikos terminus, galime pereiti tiesiai prie pagrindinės šio straipsnio temos.
Molekulinė-kinetinė teorija pasirodė ir pirmą kartą buvo suformuluota XIX amžiuje. Jo esmė slypi tame, kad jame išsamiai aprašoma bet kurios medžiagos struktūra (dažniau dujų, o ne kietų ir skystų kūnų struktūra), remiantis trimis pagrindinėmis nuostatomis, kurios buvo surinktos remiantis tokių žinomų mokslininkų kaip Robertas Hukas, Izaokas prielaidomis. Newtonas, Danielis Bernoulli, Michailas Lomonosovas ir daugelis kitų.
Pagrindinės molekulinės kinetinės teorijos nuostatos skamba taip:
- Absoliučiai visos medžiagos (nepriklausomai nuo to, ar jos skystos, kietos ar dujinės) turi sudėtingą struktūrą, susidedančią iš mažesnių dalelių: molekulių ir atomų. Atomai kartais vadinami „elementariomis molekulėmis“.
- Visos šios elementarios dalelės visada nuolat ir chaotiškai juda. Kiekvienas iš mūsų yra susidūręs su tiesioginiu šio teiginio įrodymu, bet greičiausiai neteikėme jam didelės reikšmės. Pavyzdžiui, visi matėme saulės spindulių fone, kad dulkių dalelės nuolat juda chaotiška kryptimi. Taip yra dėl to, kad atomai tarpusavyje stumia vienas kitą, nuolat perduodami kinetinę energiją vienas kitam. Šis reiškinys pirmą kartą buvo ištirtas 1827 m. ir pavadintas atradėjo vardu - „Brauno judėjimas“.
- Visos elementarios dalelės nuolat sąveikauja viena su kitatam tikros jėgos, turinčios elektrinį akmenį.
Verta pažymėti, kad kitas pavyzdys, apibūdinantis antrąją padėtį, kuris taip pat gali būti taikomas, pavyzdžiui, dujų molekulinei kinetinei teorijai, yra difuzija. Su tuo susiduriame kasdieniame gyvenime ir atliekant daugybę bandymų bei kontrolės priemonių, todėl svarbu apie tai žinoti.
Pirmiausia apsvarstykite šiuos pavyzdžius:
Gydytojas netyčia išpylė alkoholio iš kolbos ant stalo. O gal numetėte kvepalų buteliuką ir jie pasklido po visas grindis.
Kodėl šiais dviem atvejais tiek alkoholio, tiek kvepalų kvapas po kurio laiko užpildys visą kambarį, o ne tik tą vietą, kur buvo išsiliejęs šių medžiagų turinys?
Atsakymas paprastas: difuzija.
Difuzija - kas tai? Kaip tai vyksta?

Tai procesas, kurio metu dalelės, sudarančios vieną konkrečią medžiagą (dažniausiai dujas), prasiskverbia į kitos medžiagos tarpmolekulines tuštumas. Aukščiau pateiktuose pavyzdžiuose atsitiko taip: dėl terminio, tai yra nepertraukiamo ir atskirto judėjimo, alkoholio ir (arba) kvepalų molekulės pateko į tarpus tarp oro molekulių. Palaipsniui, susidūrę su oro atomais ir molekulėmis, jie pasklinda po kambarį. Beje, difuzijos intensyvumas, tai yra jos tekėjimo greitis, priklauso nuo difuzijoje dalyvaujančių medžiagų tankio, taip pat nuo jų atomų ir molekulių judėjimo energijos, vadinamos kinetine. Kuo didesnė kinetinė energija, tuo didesnis atitinkamai šių molekulių greitis ir intensyvumas.
Greičiausias difuzijos procesas gali būti vadinamas difuzija dujose. Taip yra dėl to, kad dujos savo sudėtyje nėra vienalytės, o tai reiškia, kad tarpmolekulinės tuštumos dujose užima atitinkamai daug vietos, o svetimos medžiagos atomų ir molekulių patekimo į jas procesas vyksta lengviau ir greičiau..
Šis procesas skysčiuose vyksta šiek tiek lėčiau. Cukraus kubelių ištirpimas arbatos puodelyje yra tik kietos medžiagos difuzijos skystyje pavyzdys.
Tačiau ilgiausias laikas yra difuzija kietos kristalinės struktūros kūnuose. Taip yra būtent taip, nes kietųjų kūnų struktūra yra vienalytė ir turi stiprią kristalinę gardelę, kurios ląstelėse vibruoja kietosios medžiagos atomai. Pavyzdžiui, jei dviejų metalinių strypų paviršiai bus gerai nuvalyti ir tada susiliečia vienas su kitu, tada po pakankamai ilgo laiko galėsime aptikti vieno metalo gabalus kitame ir atvirkščiai.
Kaip ir bet kuri kita esminė dalis, pagrindinė fizikos teorija suskirstyta į atskiras dalis: klasifikaciją, tipus, formules, lygtis ir pan. Taigi, mes išmokome molekulinės kinetinės teorijos pagrindus. Tai reiškia, kad galite saugiai pereiti prie atskirų teorinių blokų svarstymo.
Molekulinė-kinetinė dujų teorija
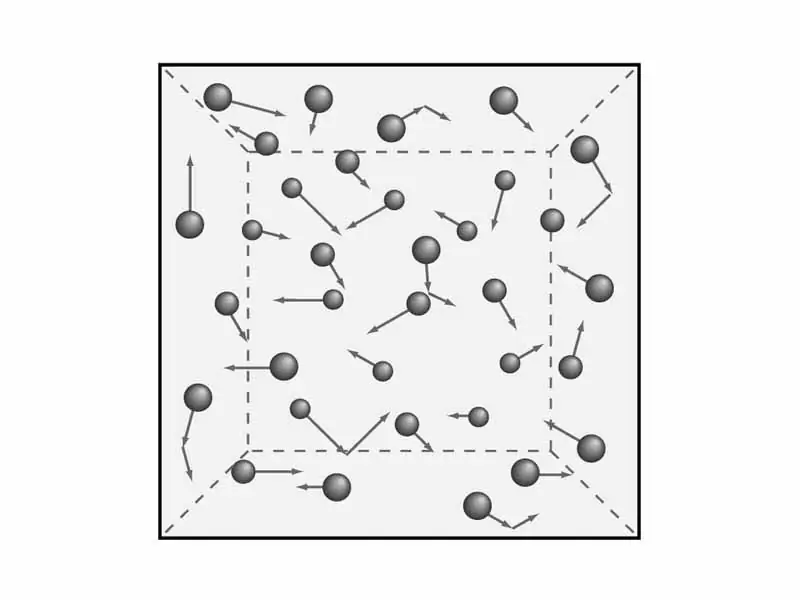
Reikia suprasti dujų teorijos nuostatas. Kaip minėjome anksčiau, apsvarstysime makroskopines dujų charakteristikas, tokias kaip slėgis ir temperatūra. Tai yravėliau prireiks, norint gauti dujų molekulinės-kinetinės teorijos lygtį. Bet matematika - vėliau, o dabar panagrinėkime teoriją ir atitinkamai fiziką.
Mokslininkai suformulavo penkias dujų molekulinės teorijos nuostatas, kurios padeda suprasti kinetinį dujų modelį. Jie skamba taip:
- Visos dujos yra sudarytos iš elementariųjų dalelių, kurios neturi tam tikro dydžio, bet turi tam tikrą masę. Kitaip tariant, šių dalelių tūris yra minimalus, palyginti su ilgiu tarp jų.
- Dujų atomai ir molekulės praktiškai neturi potencialios energijos, atitinkamai pagal dėsnį visa energija lygi kinetinei.
- Su šia pozicija jau susipažinome anksčiau - Brauno judesys. Tai reiškia, kad dujų dalelės visada nuolat ir chaotiškai juda.
- Absoliučiai visi abipusiai dujų dalelių susidūrimai, lydimi greičio ir energijos žinutės, yra visiškai elastingi. Tai reiškia, kad susidūrimo metu nėra energijos praradimo ar staigių jų kinetinės energijos šuolių.
- Esant normalioms sąlygoms ir pastoviai temperatūrai, vidutinė beveik visų dujų dalelių judėjimo energija yra vienoda.
Galime perrašyti penktąją poziciją naudodami tokio tipo dujų molekulinės-kinetinės teorijos lygtį:
E=1/2mv^2=3/2kT, kur k yra Boltzmanno konstanta; T - temperatūra kelvinais.
Ši lygtis leidžia suprasti ryšį tarp elementariųjų dujų dalelių greičio ir jų absoliučios temperatūros. Atitinkamai, kuo didesnis jų absoliutustuo didesnis jų greitis ir kinetinė energija.
Dujų slėgis
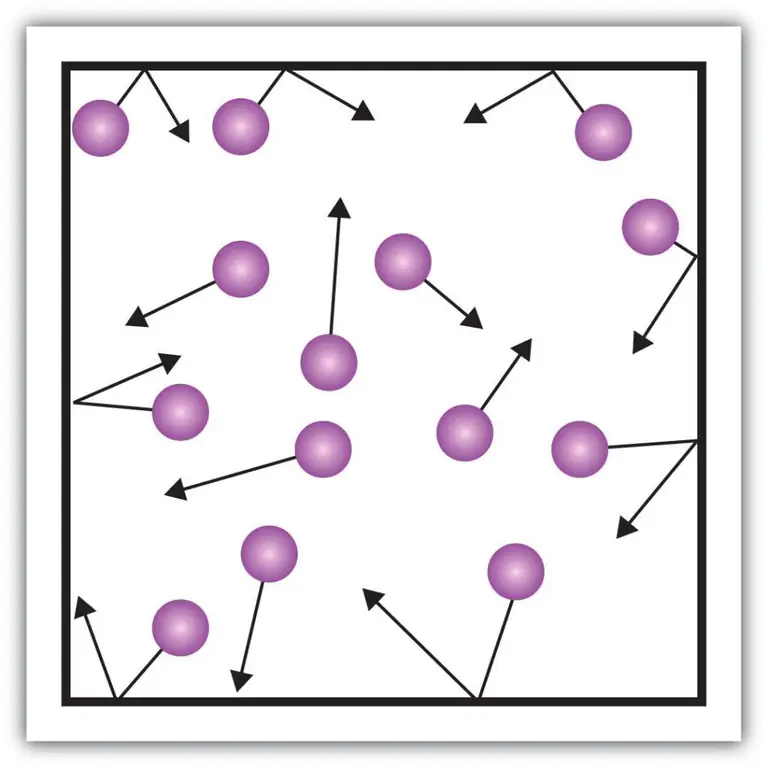
Tokius makroskopinius charakteristikos komponentus, tokius kaip dujų slėgis, taip pat galima paaiškinti naudojant kinetinę teoriją. Norėdami tai padaryti, įsivaizduokime šį pavyzdį.
Tarkime, kad kažkokių dujų molekulė yra dėžutėje, kurios ilgis yra L. Pasinaudokime aukščiau aprašytomis dujų teorijos nuostatomis ir atsižvelgsime į tai, kad molekulinė sfera juda tik išilgai x - ašis. Taigi galėsime stebėti elastinio susidūrimo su viena iš indo sienelių (dėžutės) procesą.
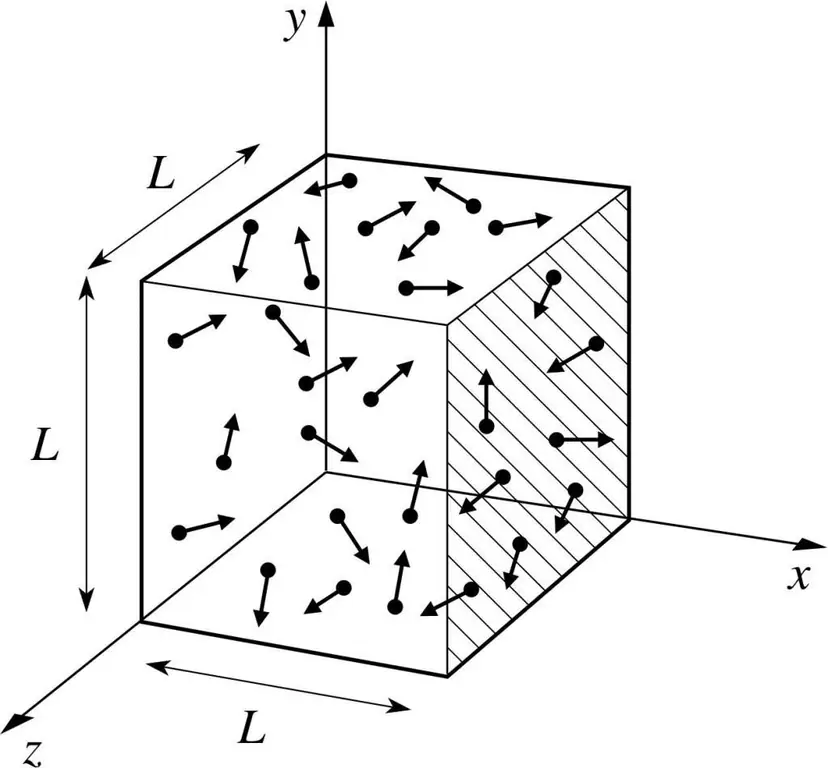
Vykstančio susidūrimo impulsas, kaip žinome, nustatomas pagal formulę: p=mv, tačiau šiuo atveju ši formulė įgis projekcijos formą: p=mv(x).
Kadangi atsižvelgiame tik į x ašies matmenį, tai yra į x ašį, visas impulso pokytis bus išreikštas formule: mv(x) - m(-v(x))=2mv(x).
Toliau pagal antrąjį Niutono dėsnį apsvarstykite mūsų objekto jėgą: F=ma=P/t.
Iš šių formulių išreiškiame slėgį iš dujų pusės: P=F/a;
Dabar pakeiskime jėgos išraišką gauta formule ir gaukime: P=mv(x)^2/L^3.
Po to mūsų paruoštą slėgio formulę galima parašyti N-ajam dujų molekulių skaičiui. Kitaip tariant, jis atrodys taip:
P=Nmv(x)^2/V, kur v - greitis, o V - tūris.
Dabar pabandykime pabrėžti keletą pagrindinių dujų slėgio nuostatų:
- Tai pasireiškia permolekulių susidūrimai su objekto, kuriame jis yra, sienų molekulėmis.
- Slėgio dydis yra tiesiogiai proporcingas molekulių smūgio į indo sieneles jėgai ir greičiui.
Trumpos išvados apie teoriją
Prieš eidami toliau ir apsvarstydami pagrindinę molekulinės kinetinės teorijos lygtį, siūlome keletą trumpų išvadų iš aukščiau pateiktų punktų ir teorijos:
- Jo atomų ir molekulių vidutinės judėjimo energijos matas yra absoliuti temperatūra.
- Kai dvi skirtingos dujos yra tos pačios temperatūros, jų molekulių vidutinė kinetinė energija yra vienoda.
- Dujų dalelių energija yra tiesiogiai proporcinga vidutiniam kvadratiniam greičiui: E=1/2mv^2.
- Nors dujų molekulės turi atitinkamai vidutinę kinetinę energiją ir vidutinį greitį, atskiros dalelės juda skirtingu greičiu: vienos greitai, kitos lėtai.
- Kuo aukštesnė temperatūra, tuo didesnis molekulių greitis.
- Kiek kartų padidiname dujų temperatūrą (pavyzdžiui, dvigubai), tiek kartų (atitinkamai padvigubėja) padidėja jų dalelių judėjimo energija.
Pagrindinė lygtis ir formulės

Pagrindinė molekulinės kinetinės teorijos lygtis leidžia nustatyti ryšį tarp mikropasaulio dydžių ir atitinkamai makroskopinių, tai yra išmatuotų, dydžių.
Vienas iš paprasčiausių modelių, kurį gali apsvarstyti molekulinė teorija, yra idealus dujų modelis.
Galima taip sakytitai tam tikras įsivaizduojamas modelis, tiriamas pagal idealių dujų molekulinę kinetinę teoriją, kurioje:
- paprasčiausios dujų dalelės laikomos tobulai elastingais kamuoliukais, kurie sąveikauja tiek tarpusavyje, tiek su bet kurio indo sienelių molekulėmis tik vienu atveju - absoliučiai tampriu susidūrimu;
- traukos jėgų dujų viduje nėra arba jos gali būti nepaisomos;
- vidinės dujų struktūros elementai gali būti laikomi materialiais taškais, tai yra, jų tūrio taip pat galima nepaisyti.
Atsižvelgdamas į tokį modelį, vokiečių kilmės fizikas Rudolfas Clausius parašė dujų slėgio formulę per mikro ir makroskopinių parametrų ryšį. Atrodo taip:
p=1/3m(0)nv^2.
Vėliau ši formulė bus vadinama pagrindine idealių dujų molekulinės-kinetinės teorijos lygtimi. Jis gali būti pateiktas keliomis skirtingomis formomis. Dabar mūsų pareiga yra parodyti tokias dalis kaip molekulinė fizika, molekulinė kinetinė teorija, taigi ir visas jų lygtis bei tipus. Todėl prasminga apsvarstyti kitus pagrindinės formulės variantus.
Žinome, kad vidutinę energiją, apibūdinančią dujų molekulių judėjimą, galima rasti naudojant formulę: E=m(0)v^2/2.
Šiuo atveju pradinėje slėgio formulėje išraišką m(0)v^2 galime pakeisti vidutine kinetine energija. Dėl to turėsime galimybę sudaryti pagrindinę dujų molekulinės kinetinės teorijos lygtį tokia forma: p=2/3nE.
Be to, visi žinome, kad išraišką m(0)n galima parašyti kaip dviejų koeficientų sandaugą:
m/NN/V=m/V=ρ.
Po šių manipuliacijų galime perrašyti idealių dujų molekulinės-kinetinės teorijos lygties formulę trečia, kita forma:
p=1/3ρv^2.
Na, galbūt tai viskas, ką jums reikia žinoti šia tema. Belieka tik susisteminti įgytas žinias trumpų (ir ne tokių) išvadų forma.
Visos bendros išvados ir formulės tema "Molekulinė-kinetinė teorija"
Taigi pradėkime.
Pirma:
Fizika yra fundamentinis mokslas, įtrauktas į gamtos mokslų kursą, tiriantis materijos ir energijos savybes, jų struktūrą, neorganinės gamtos modelius.
Ją sudaro šie skyriai:
- mechanika (kinematika ir dinamika);
- statinis;
- termodinamika;
- elektrodinamika;
- molekulinė pjūvis;
- optika;
- kvantų ir atomo branduolio fizika.
Antra:
Dalelių fizika ir termodinamika yra glaudžiai susijusios šakos, tiriančios išskirtinai makroskopinį viso fizinių sistemų skaičiaus komponentą, ty sistemas, susidedančias iš daugybės elementariųjų dalelių.
Jie pagrįsti molekuline kinetikos teorija.
Trečia:
Klausimo esmė yra tokia. Molekulinė kinetinė teorija detaliai aprašo medžiagos sandarą (dažniau dujų, o ne kietųjų medžiagų struktūrą).ir skysti kūnai), remiantis trimis pagrindinėmis prielaidomis, kurios buvo surinktos iš žinomų mokslininkų prielaidų. Tarp jų: Robertas Hukas, Isaacas Newtonas, Danielis Bernoulli, Michailas Lomonosovas ir daugelis kitų.
Ketvirta:
Trys pagrindiniai molekulinės kinetinės teorijos principai:
- Visos medžiagos (nepriklausomai nuo to, ar jos skystos, kietos ar dujinės) turi sudėtingą struktūrą, kurią sudaro mažesnės dalelės: molekulės ir atomai.
- Visos šios paprastos dalelės nuolat chaotiškai juda. Pavyzdys: Brauno judėjimas ir difuzija.
- Visos molekulės bet kokiomis sąlygomis sąveikauja viena su kita su tam tikromis jėgomis, turinčiomis elektrinę uolieną.
Kiekviena iš šių molekulinės kinetinės teorijos nuostatų yra tvirtas materijos struktūros tyrimo pagrindas.
Penkta:
Keli pagrindiniai dujų modelio molekulinės teorijos punktai:
- Visos dujos yra sudarytos iš elementariųjų dalelių, kurios neturi tam tikro dydžio, bet turi tam tikrą masę. Kitaip tariant, šių dalelių tūris yra minimalus, palyginti su atstumais tarp jų.
- Dujų atomai ir molekulės praktiškai neturi potencialios energijos, atitinkamai jų bendra energija lygi kinetinei.
- Su šia pozicija jau susipažinome anksčiau - Brauno judesys. Tai reiškia, kad dujų dalelės visada nuolat ir atsitiktinai juda.
- Absoliučiai visi tarpusavio atomų ir dujų molekulių susidūrimai, lydimi greičio ir energijos pranešimo, yra visiškai elastingi. Tai yrareiškia, kad susidūrimo metu nėra energijos praradimo ar staigių kinetinės energijos šuolių.
- Esant normalioms sąlygoms ir pastoviai temperatūrai, beveik visų dujų vidutinė kinetinė energija yra vienoda.
Šešta:
Išvados iš teorijos apie dujas:
- Absoliuti temperatūra yra jos atomų ir molekulių vidutinės kinetinės energijos matas.
- Kai dvi skirtingos dujos yra tos pačios temperatūros, jų molekulių vidutinė kinetinė energija yra vienoda.
- Vidutinė dujų dalelių kinetinė energija yra tiesiogiai proporcinga vidutiniam kvadratiniam greičiui: E=1/2mv^2.
- Nors dujų molekulės turi atitinkamai vidutinę kinetinę energiją ir vidutinį greitį, atskiros dalelės juda skirtingu greičiu: vienos greitai, kitos lėtai.
- Kuo aukštesnė temperatūra, tuo didesnis molekulių greitis.
- Kiek kartų padidiname dujų temperatūrą (pavyzdžiui, dvigubai), tiek kartų (atitinkamai padvigubėja) padidėja ir vidutinė jų dalelių kinetinė energija.
- Ryšys tarp dujų slėgio ant indo, kuriame jos yra, sieneles ir molekulių poveikio šioms sienelėms intensyvumo yra tiesiogiai proporcingas: kuo daugiau smūgių, tuo didesnis slėgis ir atvirkščiai..
Septinta:
Idealus dujų modelis - tai modelis, kuriame turi būti įvykdytos šios sąlygos:
- Dujų molekulės gali ir yra laikomos tobulai elastingais rutuliais.
- Šie rutuliai gali sąveikauti vienas su kitu ir su bet kurios sienos sienomislaivas tik vienu atveju - absoliučiai elastingas susidūrimas.
- Tų jėgų, kurios apibūdina abipusę dujų atomų ir molekulių trauką, nėra arba jų galima nepaisyti.
- Atomai ir molekulės laikomi materialiais taškais, tai yra, jų tūrio taip pat galima nepaisyti.
Aštuntasis:
Pateikime visas pagrindines lygtis ir parodykime formules temoje "Molekulinė-kinetinė teorija":
p=1/3m(0)nv^2 - pagrindinė idealių dujų modelio lygtis, kurią išvedė vokiečių fizikas Rudolfas Clausius.
p=2/3nE - pagrindinė idealių dujų molekulinės-kinetinės teorijos lygtis. Išvesta iš vidutinės molekulių kinetinės energijos.
р=1/3ρv^2 - ta pati lygtis, bet atsižvelgiama į idealių dujų molekulių tankį ir vidutinį kvadratinį greitį.
m(0)=M/N(a) - formulė, kaip rasti vienos molekulės masę pagal Avogadro skaičių.
v^2=(v(1)+v(2)+v(3)+…)/N - molekulių vidutinio kvadratinio greičio nustatymo formulė, kur v(1), v(2), v (3) ir tt - pirmosios molekulės greitis, antroji, trečioji ir taip toliau iki n-osios molekulės.
n=N/V - molekulių koncentracijos nustatymo formulė, kur N yra molekulių skaičius dujų tūryje iki nurodyto tūrio V.
E=mv^2/2=3/2kT - vidutinės molekulių kinetinės energijos nustatymo formulės, kur v^2 - molekulių vidutinis kvadratinis greitis, k - konstanta vertė, pavadinta austro Ludwigo Boltzmanno fizikos vardu, o T yra dujų temperatūra.
p=nkT - slėgio formulė pagal koncentraciją, pastoviBoltzmannas ir absoliuti temperatūra T. Iš jos išplaukia kita esminė formulė, kurią atrado rusų mokslininkas Mendelejevas ir prancūzų fizikas inžinierius Klaiperonas:
pV=m/MRT, kur R=kN(a) yra universali dujų konstanta.
Dabar parodykime skirtingų izoprocesų konstantas: izobarinį, izochorinį, izoterminį ir adiabatinį.
pV/T=const - atliekama, kai dujų masė ir sudėtis yra pastovios.
рV=const - jei temperatūra taip pat pastovi.
V/T=const - jei dujų slėgis pastovus.
p/T=const - jei garsumas pastovus.
Galbūt tai viskas, ką reikia žinoti šia tema.
Šiandien mes pasinėrėme į tokią mokslo sritį kaip teorinė fizika, daugybė jos skyrių ir blokų. Išsamiau palietėme tokią fizikos sritį kaip pagrindinė molekulinė fizika ir termodinamika, būtent molekulinė-kinetinė teorija, kuri, atrodo, nesukelia jokių sunkumų pradiniame tyrime, tačiau iš tikrųjų turi daug spąstų.. Tai praplečia mūsų supratimą apie idealių dujų modelį, kurį taip pat išsamiai ištyrėme. Be to, verta paminėti, kad mes taip pat susipažinome su pagrindinėmis molekulinės teorijos lygtimis įvairiomis jų variacijomis, taip pat apsvarstėme visas būtiniausias formules ieškant tam tikrų nežinomų dydžių šia tema. Tai bus ypač naudinga ruošiantis rašyti bet kokius testus, egzaminus ir testus arba išplėsti bendrą fizikos perspektyvą ir žinias.
Tikimės, kad šis straipsnis jums buvo naudingas ir iš jo ištraukėte tik būtiniausią informaciją, sustiprindami savo žinias apie tokius termodinamikos ramsčius kaip pagrindinės molekulinės kinetinės teorijos nuostatos.






