Dujos termodinamikos požiūriu apibūdinamos makroskopinių charakteristikų visuma, iš kurių pagrindinės yra temperatūra, slėgis ir tūris. Vieno iš šių parametrų pastovumas ir kitų dviejų pokytis rodo, kad dujose vyksta vienoks ar kitoks izoprocesas. Šį straipsnį skirsime išsamiam atsakymui į klausimus, kad tai izochorinis procesas, kuo jis skiriasi nuo izoterminių ir izobarinių dujų sistemos būsenų pokyčių.
Idealios dujos fizikoje

Prieš atsakydami į klausimą, kad tai izochorinis procesas, turėtumėte geriau susipažinti su idealių dujų sąvoka. Fizikoje tai suprantama kaip bet kurios dujos, kuriose jas sudarančių dalelių vidutinė kinetinė energija gerokai viršija potencialią jų sąveikos energiją, o atstumai tarp šių dalelių yra keliomis eilėmis didesni už jų linijinius matmenis. Esant nurodytoms sąlygoms, tai įmanoma atliekantskaičiavimuose neatsižvelgiama į sąveikos energiją tarp dalelių (ji lygi nuliui), taip pat galima daryti prielaidą, kad dalelės yra materialūs taškai, turintys tam tikrą masę m.
Vienintelis procesas, vykstantis idealiose dujose, yra dalelių susidūrimas su indo, kuriame yra medžiaga, sienelėmis. Šie susidūrimai praktiškai pasireiškia kaip tam tikro slėgio buvimas dujose P.
Paprastai bet kuri dujinė medžiaga, kurią sudaro santykinai chemiškai inertiškos molekulės ir kurios turi žemą slėgį bei aukštą temperatūrą, gali būti laikomos idealiomis dujomis, kurių tikslumas yra pakankamas praktiniams skaičiavimams.
Idealias dujas apibūdinanti lygtis
Žinoma, mes kalbame apie universalų Clapeyrono-Mendelejevo dėsnį, kurį reikėtų gerai suprasti, kad suprastume, jog tai izochorinis procesas. Taigi, visuotinė būsenos lygtis turi tokią formą:
PV=nRT.
Tai yra, slėgio P ir dujų tūrio V sandauga yra lygi absoliučios temperatūros T sandaugai ir medžiagos kiekiui moliais n, kur R yra proporcingumo koeficientas. Pačią lygtį 1834 m. pirmą kartą užrašė Emile'as Clapeyronas, o 19 amžiaus aštuntajame dešimtmetyje D. Mendelejevas joje pakeitė vienos universalios dujų konstantos R (8,314 J/(molK) pastovių verčių rinkinį.)).
Pagal Clapeyrono-Mendelejevo lygtį, uždaroje sistemoje dujų dalelių skaičius išlieka pastovus, todėl yra tik trys makroskopiniai parametrai, kurie gali keistis (T, Pir V). Pastarasis faktas leidžia suprasti įvairius izoprocesus, kurie bus aptarti toliau.
Kas yra izochorinis procesas?
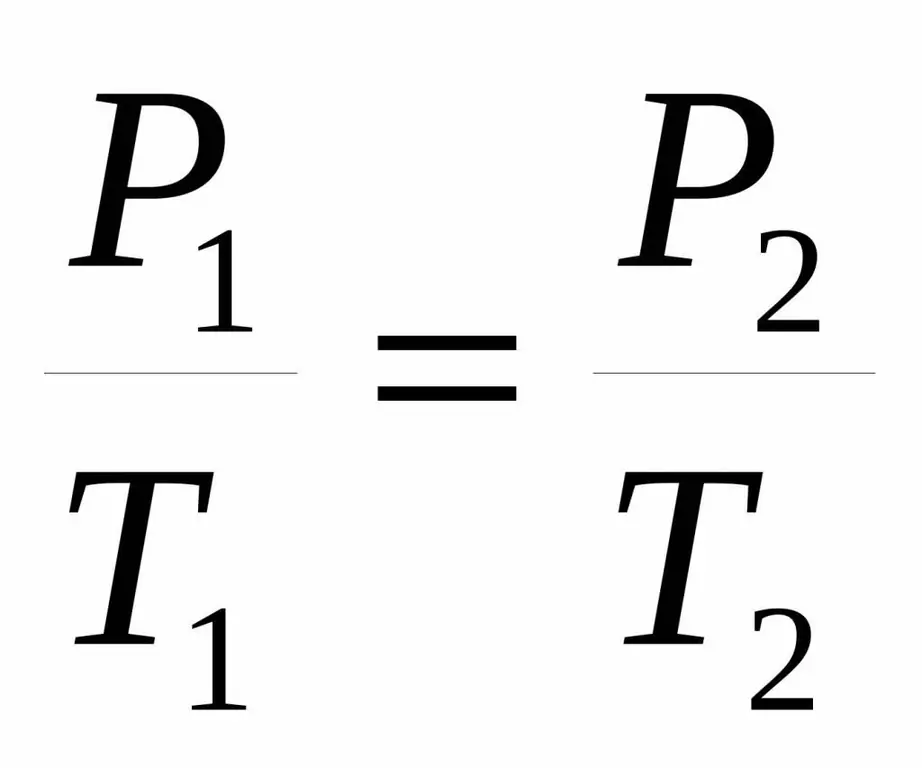
Šis procesas suprantamas kaip absoliučiai bet koks sistemos būsenos pokytis, kuriame išsaugomas jos tūris.
Jei pereitume prie universalios būsenos lygties, galime pasakyti, kad izochoriniame procese dujose kinta tik slėgis ir absoliuti temperatūra. Norėdami tiksliai suprasti, kaip keičiasi termodinaminiai parametrai, parašome atitinkamą matematinę išraišką:
P / T=konst.
Kartais ši lygybė pateikiama šiek tiek kitokia forma:
P1 / T1=P2 / T 2.
Abi lygybės vadinamos Charleso dėsniu pagal prancūzų mokslininko, kuris XVIII amžiaus pabaigoje eksperimentiškai gavo pažymėtą priklausomybę, vardo.

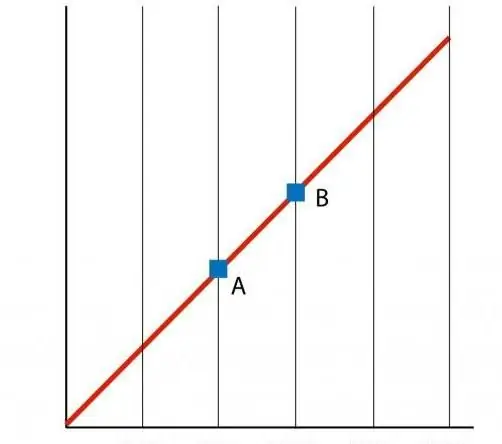
Jei sudarysime funkcijos P(T) grafiką, gausime tiesinę priklausomybę, kuri vadinama izochora. Bet kuri izochora (visoms n ir V reikšmėms) yra tiesi linija.
Energetinis proceso aprašymas
Kaip pažymėta, izochorinis procesas yra sistemos būsenos pasikeitimas, vykstantis uždaroje, bet ne izoliuotoje sistemoje. Kalbame apie šilumos mainų tarp dujų ir aplinkos galimybę. Apskritai, bet koks šilumos Q tiekimas į sistemą duoda du rezultatus:
- pakeičia vidinę energiją U;
- dujosveikia A, plečiasi arba susitraukia.
Paskutinė išvada parašyta matematiškai taip:
Q=U + A.
Idealiųjų dujų izochorinis procesas pagal savo apibrėžimą nereiškia, kad dujos atlieka darbą, nes jų tūris nesikeičia. Tai reiškia, kad visa sistemai tiekiama šiluma skirta jos vidinei energijai padidinti:
Q=U.
Jei šioje išraiškoje pakeisime aiškią vidinės energijos formulę, izochorinio proceso šilumą galima pavaizduoti taip:
Q=z / 2nRT.
Čia z yra laisvės laipsnių skaičius, kurį lemia dujas sudarančių molekulių poliatominė prigimtis. Vienatominėms dujoms z=3, dviatomėms dujoms - 5, triatomėms ir daugiau - 6. Čia, pagal laisvės laipsnius, turime omenyje transliacijos ir sukimosi laipsnius.
Jei palyginsime dujų sistemos šildymo efektyvumą izochoriniuose ir izobariniuose procesuose, tai pirmuoju atveju gausime maksimalų efektyvumą, nes izobariškai keičiantis sistemos būsenai, dujos plečiasi ir dalis šilumos išleidžiama darbui.
Izobarinis procesas
Aukščiau mes išsamiai aprašėme, kad tai izochorinis procesas. Dabar pakalbėkime keletą žodžių apie kitus izoprocesus. Pradėkime nuo izobarikos. Remiantis pavadinimu, jis suprantamas kaip sistemos perėjimas tarp būsenų esant pastoviam slėgiui. Šį procesą Gay-Lussac įstatymas apibūdina taip:
V / T=konst.
Kaip ir izochoro atveju, V(T) izobaras taip pat reiškia tiesią grafiko liniją.
Užbet kokio izobarinio proceso metu patogu apskaičiuoti dujų atliekamą darbą, nes jis lygus pastovaus slėgio ir tūrio pokyčio sandaugai.
Izoterminis procesas
Tai procesas, kurio metu sistemos temperatūra išlieka pastovi. Tai apibūdina Boyle-Mariotte dėsnis idealioms dujoms. Įdomu pastebėti, kad tai pirmasis eksperimentiškai atrastas dujų įstatymas (XVII a. antroji pusė). Jo matematinis žymėjimas atrodo taip:
PV=konst.
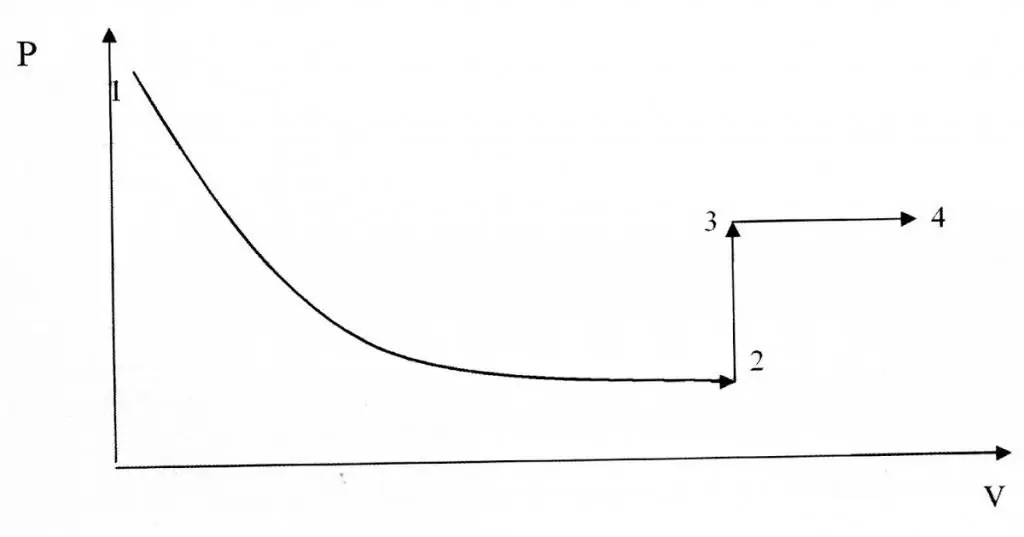
Izochoriniai ir izoterminiai procesai skiriasi savo grafiniu vaizdavimu, nes funkcija P(V) yra hiperbolinis, o ne tiesinis ryšys.
Problemos sprendimo pavyzdys
Apibendrinkime straipsnyje pateiktą teorinę informaciją jų pritaikymu praktinei problemai spręsti. Yra žinoma, kad gryno dujinio azoto balione buvo 1 atmosferos slėgis ir 25 °C temperatūra. Įkaitinus dujų balioną ir išmatavus jame esantį slėgį paaiškėjo, kad jis yra 1,5 atmosferos. Kokia yra dujų temperatūra balione po kaitinimo? Kiek pasikeitė vidinė dujų energija, jei balione buvo 4 moliai azoto.
Norėdami atsakyti į pirmąjį klausimą, naudojame šią išraišką:
P1 / T1=P2 / T 2.
Iš kur gauname:
T2=P2 / P1 T 1.
Šioje išraiškoje slėgis gali būti pakeistas savavališkais vienetaismatmenys, nes jie traukiasi, o temperatūra tik kelvinais. Tai pasakę, gauname:
T2=1,5 /1298,15=447,224 K.
Apskaičiuota temperatūra Celsijaus laipsniais yra 174 °C.
Kadangi azoto molekulė yra dviatomė, jos vidinės energijos pokytį kaitinant galima nustatyti taip:
ΔU=5 / 2nRΔT.
Pakeitę žinomas reikšmes į šią išraišką, gausime atsakymą į antrąjį problemos klausimą: ΔU=+12,4 kJ.






