Svarbi termodinamikos dalis yra transformacijų tarp skirtingų medžiagos fazių tyrimas, nes šie procesai vyksta praktiškai ir yra labai svarbūs numatant sistemos elgesį tam tikromis sąlygomis. Šios transformacijos vadinamos faziniais perėjimais, kuriems skirtas straipsnis.
Fazės ir sistemos komponento samprata

Prieš pradedant nagrinėti fazių perėjimus fizikoje, būtina apibrėžti pačios fazės sąvoką. Kaip žinoma iš bendrosios fizikos kurso, yra trys materijos būsenos: dujinė, kieta ir skysta. Specialioje mokslo dalyje - termodinamikoje - dėsniai formuluojami materijos fazėms, o ne jų agregacijos būsenoms. Fazė suprantama kaip tam tikras medžiagos tūris, turintis homogeninę struktūrą, pasižymintis specifinėmis fizinėmis ir cheminėmis savybėmis ir atskirtas nuo likusios materijos ribomis, kurios vadinamos tarpfaze.
Taigi „fazės“sąvoka turi daug praktiškesnės informacijos apie savybesmedžiaga nei jos agregacijos būsena. Pavyzdžiui, metalo, pvz., geležies, kietosios būsenos fazės: žemos temperatūros magnetinis korpuso centre (BCC), žemos temperatūros nemagnetinis bcc, į veidą orientuotas kubas (fcc) ir aukštas. temperatūros nemagnetinė bcc.
Be sąvokos „fazė“, termodinamikos dėsniuose taip pat vartojamas terminas „komponentai“, kuris reiškia cheminių elementų, sudarančių tam tikrą sistemą, skaičių. Tai reiškia, kad fazė gali būti vienakomponentė (1 cheminis elementas) arba daugiakomponentė (keli cheminiai elementai).
Gibbso teorema ir pusiausvyra tarp sistemos fazių

Norint suprasti fazių perėjimus, būtina žinoti jų pusiausvyros sąlygas. Šias sąlygas galima matematiškai gauti sprendžiant kiekvienos iš jų Gibso lygčių sistemą, darant prielaidą, kad pusiausvyros būsena pasiekiama tada, kai nustoja keistis nuo išorinio poveikio izoliuotos sistemos bendra Gibso energija.
Išsprendus nurodytą lygčių sistemą, gaunamos sąlygos pusiausvyrai tarp kelių fazių egzistuoti: izoliuota sistema nustos vystytis tik tada, kai visose fazėse atsiras slėgiai, kiekvieno komponento cheminiai potencialai ir temperatūros yra lygūs vienas kitam.
Pusiausvyros Gibso fazės taisyklė

Iš kelių fazių ir komponentų susidedanti sistema gali būti ne tik pusiausvyrojetam tikromis sąlygomis, pavyzdžiui, esant tam tikrai temperatūrai ir slėgiui. Kai kurie Gibbso teoremos kintamieji pusiausvyrai gali būti pakeisti išlaikant ir fazių skaičių, ir komponentų, kurie yra šioje pusiausvyroje, skaičių. Kintamųjų, kuriuos galima keisti nepažeidžiant pusiausvyros sistemoje, skaičius vadinamas šios sistemos laisvių skaičiumi.
Sistemos, susidedančios iš f fazių ir k komponentų, laisvių skaičius l yra vienareikšmiškai nustatomas pagal Gibso fazių taisyklę. Ši taisyklė matematiškai parašyta taip: l + f=k + 2. Kaip dirbti su šia taisykle? Labai paprasta. Pavyzdžiui, žinoma, kad sistema susideda iš f=3 pusiausvyros fazių. Koks mažiausias komponentų skaičius gali būti tokioje sistemoje? Į klausimą galite atsakyti samprotaudami taip: pusiausvyros atveju griežčiausios sąlygos yra tada, kai ji realizuojama tik esant tam tikriems rodikliams, tai yra, bet kurio termodinaminio parametro pasikeitimas sukels disbalansą. Tai reiškia, kad laisvių skaičius l=0. Pakeitus žinomas l ir f reikšmes, gauname k=1, tai yra, sistema, kurioje trys fazės yra pusiausvyroje, gali būti sudaryta iš vieno komponento. Puikus pavyzdys yra trigubas vandens taškas, kuriame ledas, skystas vanduo ir garai egzistuoja pusiausvyroje esant tam tikrai temperatūrai ir slėgiui.
Fazinių transformacijų klasifikacija
Jei pradėsite keisti kai kuriuos termodinaminius parametrus pusiausvyroje esančioje sistemoje, galite stebėti, kaip viena fazė išnyks ir atsiras kita. Paprastas šio proceso pavyzdys - ledo tirpimas jį kaitinant.
Atsižvelgiant į tai, kad Gibso lygtis priklauso tik nuo dviejų kintamųjų (slėgio ir temperatūros), o fazinis perėjimas susijęs su šių kintamųjų pasikeitimu, matematiškai perėjimą tarp fazių galima apibūdinti diferencijuojant Gibso energiją jos atžvilgiu. kintamieji. Būtent šį metodą 1933 m. naudojo austrų fizikas Paulas Ehrenfestas, sudaręs visų žinomų termodinaminių procesų, vykstančių pasikeitus fazių pusiausvyrai, klasifikaciją.
Iš termodinamikos pagrindų išplaukia, kad pirmoji Gibso energijos išvestinė temperatūros atžvilgiu yra lygi sistemos entropijos pokyčiui. Gibso energijos išvestinė slėgio atžvilgiu yra lygi tūrio pokyčiui. Jei, pasikeitus sistemos fazėms, entropija arba tūris nutrūksta, tai yra, jie staigiai keičiasi, tada jie kalba apie pirmos eilės fazių perėjimą.
Be to, antrosios Gibso energijos išvestinės temperatūros ir slėgio atžvilgiu yra atitinkamai šiluminė talpa ir tūrio plėtimosi koeficientas. Jei transformaciją tarp fazių lydi nurodytų fizikinių dydžių verčių nepertraukiamumas, tada kalbama apie antros eilės fazių perėjimą.
Transformacijų tarp fazių pavyzdžiai

Gamtoje yra daugybė skirtingų perėjimų. Šioje klasifikacijoje ryškūs pirmojo tipo perėjimų pavyzdžiai yra metalų lydymosi procesai arba vandens garų kondensacija iš oro, kai sistemoje vyksta tūrio šuolis.
Jei kalbėtume apie antros eilės perėjimus, ryškūs pavyzdžiai yra geležies transformacija iš magnetinės į paramagnetinę būseną esant temperatūrai768 ºC arba metalinio laidininko pavertimas superlaidžia būsena, esant temperatūrai, artimai absoliučiam nuliui.
Lygtys, apibūdinančios pirmos rūšies perėjimus
Praktikoje dažnai reikia žinoti, kaip sistemoje kinta temperatūra, slėgis ir sugerta (išleidžiama) energija, kai joje vyksta fazinės transformacijos. Tam naudojamos dvi svarbios lygtys. Jie gauti remiantis termodinamikos pagrindų žiniomis:
- Clapeyrono formulė, kuri nustato ryšį tarp slėgio ir temperatūros transformuojant tarp skirtingų fazių.
- Klausiaus formulė, kuri susieja absorbuotą (išleidžiamą) energiją ir sistemos temperatūrą transformacijos metu.
Abi lygtys naudojamos ne tik norint gauti kiekybines fizikinių dydžių priklausomybes, bet ir nustatyti fazių diagramų pusiausvyros kreivių nuolydžio ženklą.
Antrojo tipo perėjimų apibūdinimo lygtis

1-ojo ir 2-ojo tipo fazių perėjimai aprašomi skirtingomis lygtimis, nes Clausius ir Clausius lygčių taikymas antros eilės perėjimams sukelia matematinį neapibrėžtumą.
Pastarajam apibūdinti naudojamos Erenfesto lygtys, kurios nustato ryšį tarp slėgio ir temperatūros pokyčių, žinant apie šilumos talpos pokyčius ir tūrio plėtimosi koeficientą transformacijos proceso metu. Erenfesto lygtys naudojamos laidininko ir superlaidininko perėjimams apibūdinti, kai nėra magnetinio lauko.
Svarbafazių diagramos
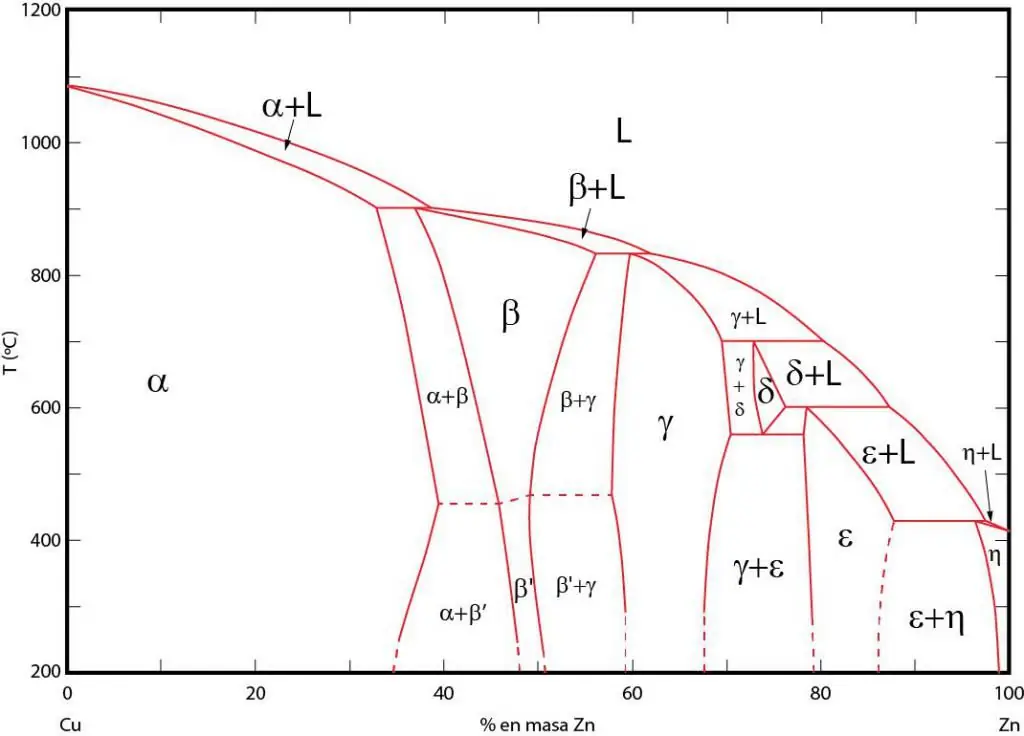
Fazių diagramos yra grafinis sričių, kuriose atitinkamos fazės egzistuoja pusiausvyroje, vaizdas. Šios sritys yra atskirtos pusiausvyros linijomis tarp fazių. Dažnai naudojamos P-T (slėgis-temperatūra), T-V (temperatūra-tūris) ir P-V (slėgis-tūris) fazių diagramos.
Fazinių diagramų svarba slypi tame, kad jos leidžia numatyti, kokioje fazėje bus sistema, atitinkamai pasikeitus išorinėms sąlygoms. Ši informacija naudojama termiškai apdorojant įvairias medžiagas, siekiant gauti norimų savybių struktūrą.






