Tiriant dujų elgseną fizikoje daug dėmesio skiriama izoprocesams, tai yra tokiems perėjimams tarp sistemos būsenų, kurių metu išsaugomas vienas termodinaminis parametras. Tačiau tarp būsenų vyksta dujų perėjimas, kuris nėra izoprocesas, bet atlieka svarbų vaidmenį gamtoje ir technologijoje. Tai adiabatinis procesas. Šiame straipsnyje mes jį apsvarstysime išsamiau, sutelkdami dėmesį į tai, kas yra dujų adiabatinis eksponentas.
Adiabatinis procesas
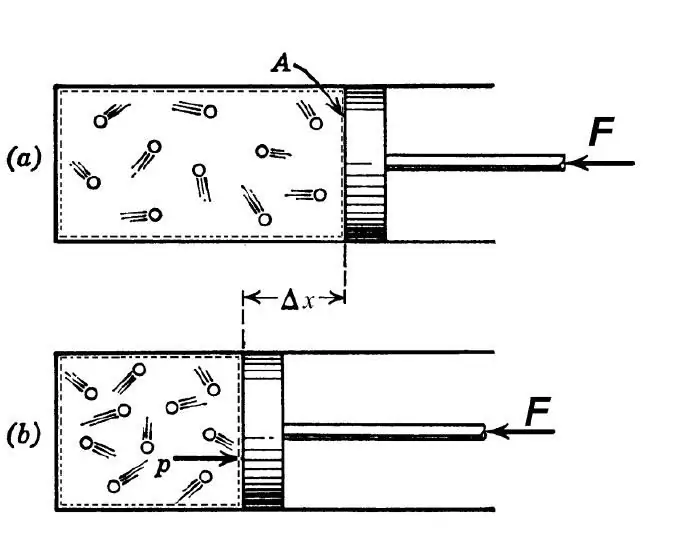
Pagal termodinaminį apibrėžimą adiabatinis procesas suprantamas kaip toks perėjimas tarp pradinės ir galutinės sistemos būsenų, dėl kurio nevyksta šilumos mainai tarp išorinės aplinkos ir tiriamos sistemos. Toks procesas galimas esant dviem sąlygoms:
- šilumos laidumas tarp išorinės aplinkos irsistema yra žema dėl vienos ar kitos priežasties;
- proceso greitis didelis, todėl šilumos mainai nespėja įvykti.
Inžinerijos srityje adiabatinis perėjimas naudojamas dujoms pašildyti staigiai suspaudžiant ir aušinti, kai jos greitai plečiasi. Gamtoje aptariamas termodinaminis perėjimas pasireiškia tada, kai oro masė kyla arba leidžiasi žemyn nuo kalno šlaito. Dėl tokių pakilimų ir nuosmukių keičiasi oro rasos taškas ir iškrenta krituliai.
Puasono lygtis idealiosioms adiabatinėms dujoms

Idealios dujos yra sistema, kurioje dalelės juda atsitiktinai dideliu greičiu, nesąveikauja viena su kita ir yra be matmenų. Toks modelis yra labai paprastas matematiniu apibūdinimu.
Pagal adiabatinio proceso apibrėžimą, pagal pirmąjį termodinamikos dėsnį galima parašyti tokią išraišką:
dU=-PdV.
Kitaip tariant, dujos, besiplečiančios arba susitraukusios, veikia PdV dėl atitinkamo jų vidinės energijos dU pasikeitimo.
Idealiųjų dujų atveju, jei naudosime būsenos lygtį (Clapeyrono-Mendelejevo dėsnis), galime gauti tokią išraišką:
PVγ=const.
Ši lygybė vadinama Puasono lygtimi. Žmonės, kurie yra susipažinę su dujų fizika, pastebės, kad jei γ reikšmė lygi 1, tada Puasono lygtis pateks į Boyle-Mariotte dėsnį (izoterminėprocesas). Tačiau toks lygčių transformavimas neįmanomas, nes γ bet kokio tipo idealioms dujoms yra didesnis už vieną. Dydis γ (gama) vadinamas idealių dujų adiabatiniu indeksu. Pažvelkime atidžiau į jo fizinę reikšmę.
Kas yra adiabatinis eksponentas?
Rodiklis γ, rodomas Puasono lygtyje idealioms dujoms, yra pastovaus slėgio šiluminės talpos santykis su ta pačia verte, bet jau esant pastoviam tūriui. Fizikoje šiluminė talpa yra šilumos kiekis, kuris turi būti perduotas arba paimtas iš tam tikros sistemos, kad ji pakeistų savo temperatūrą 1 Kelvinu. Izobarinę šiluminę talpą žymėsime simboliu CP, o izochorinę šiluminę talpą - simboliu CV. Tada lygybė galioja γ:
γ=CP/CV.
Kadangi γ visada didesnis už vienetą, tai rodo, kiek kartų tiriamos dujų sistemos izobarinė šiluminė talpa viršija panašią izochorinę charakteristiką.
CP ir CV šiluminės galios
Norint nustatyti adiabatinį eksponentą, reikia gerai suprasti dydžių CP ir CV reikšmę. Norėdami tai padaryti, atliksime tokį minties eksperimentą: įsivaizduokite, kad dujos yra uždaroje sistemoje inde su kietomis sienelėmis. Jei indas yra šildomas, visa perduodama šiluma idealiu atveju bus paversta vidine dujų energija. Esant tokiai situacijai, galios lygybė:
dU=CVdT.
VertėCV apibrėžia šilumos kiekį, kuris turi būti perduotas į sistemą, kad ji izochoriškai pašildytų 1 K.
Dabar tarkime, kad dujos yra inde su judančiu stūmokliu. Šildant tokią sistemą, stūmoklis judės, užtikrindamas pastovų slėgį. Kadangi sistemos entalpija šiuo atveju bus lygi izobarinės šiluminės talpos ir temperatūros pokyčio sandaugai, pirmasis termodinamikos dėsnis bus toks:
CPdT=CVdT + PdV.
Iš čia matyti, kad CP>CV, kadangi izobarinio būsenų kaitos atveju būtina išleisti šilumą ne tik sistemos temperatūrai padidinti, taigi ir jos vidinei energijai, bet ir dujų atliekamam darbui plečiant.
γ vertė idealioms monoatominėms dujoms
Paprasčiausia dujų sistema yra monoatominės idealios dujos. Tarkime, kad turime 1 molį tokių dujų. Prisiminkite, kad 1 mol dujų izobarinio kaitinimo procese tik 1 kelvinu jis veikia lygus R. Šis simbolis dažniausiai naudojamas visuotinei dujų konstantai žymėti. Jis lygus 8 314 J / (molK). Taikant paskutinę išraišką ankstesnėje pastraipoje šiuo atveju, gauname tokią lygybę:
CP=CV+ R.
Iš kur galite nustatyti izochorinės šilumos talpos vertę CV:
γ=CP/CV;
CV=R/(γ-1).
Žinoma, kad vienam kurmiuimonoatominės dujos, izochorinės šiluminės talpos vertė yra:
CV=3/2R.
Iš paskutinių dviejų lygčių seka adiabatinio eksponento reikšmė:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Atkreipkite dėmesį, kad γ reikšmė priklauso tik nuo vidinių pačių dujų savybių (nuo jų molekulių daugiaatomiškumo) ir nepriklauso nuo medžiagos kiekio sistemoje.
γ priklausomybė nuo laisvės laipsnių skaičiaus
Monatominių dujų izochorinės šiluminės talpos lygtis buvo parašyta aukščiau. Jame pasirodęs koeficientas 3/2 yra susijęs su vieno atomo laisvės laipsnių skaičiumi. Jis turi galimybę judėti tik viena iš trijų erdvės krypčių, tai yra, yra tik transliaciniai laisvės laipsniai.
Jei sistemą sudaro dviatomės molekulės, tada prie trijų transliacinių laipsnių pridedami dar du sukimosi laipsniai. Todėl CV išraiška tampa:
CV=5/2R.
Tada γ reikšmė bus:
γ=7/5=1, 4.
Atkreipkite dėmesį, kad dviatomė molekulė iš tikrųjų turi dar vieną virpesių laisvės laipsnį, tačiau esant kelių šimtų kelvinų temperatūrai, ji nėra aktyvuojama ir nepadidina šiluminės talpos.
Jei dujų molekulės susideda iš daugiau nei dviejų atomų, tada jos turės 6 laisvės laipsnius. Adiabatinis eksponentas šiuo atveju bus lygus:
γ=4/3 ≈ 1, 33.
TaigiTaigi, didėjant atomų skaičiui dujų molekulėje, γ reikšmė mažėja. Jei sukursite adiabatinį grafiką P-V ašyse, pastebėsite, kad monoatominių dujų kreivė elgsis ryškesnė nei daugiaatomės.
Dujų mišinio adiabatinis eksponentas
Aukščiau parodėme, kad γ reikšmė nepriklauso nuo dujų sistemos cheminės sudėties. Tačiau tai priklauso nuo atomų, sudarančių jo molekules, skaičiaus. Tarkime, kad sistema susideda iš N komponentų. Komponento i atominė dalis mišinyje yra ai. Tada, norėdami nustatyti mišinio adiabatinį eksponentą, galite naudoti šią išraišką:
γ=∑i=1N(aiγ i).
Kur γi yra i-ojo komponento γ reikšmė.
Pavyzdžiui, ši išraiška gali būti naudojama norint nustatyti oro γ. Kadangi jį sudaro 99 % dviatomių deguonies ir azoto molekulių, jo adiabatinis indeksas turėtų būti labai artimas 1,4 vertei, o tai patvirtina eksperimentinis šios vertės nustatymas.






